Estructura de Lewis y su importancia para la química

Si el objetivo de la educación infantil es ser a la vez base y eslabón para el resto del proceso educativo, deberá asegurarse de formar competencias y habilidades en gran parte de las áreas de conocimiento. Dicho esto, aunque las competencias químicas se desarrollan en forma en la educación secundaria, se pueden establecer los inicios de las relaciones científicas desde las primeras estancias de la educación y para esto es fundamental conocerlo todo sobre la estructura de Lewis.
Cuál es la estructura de Lewis y para qué sirve
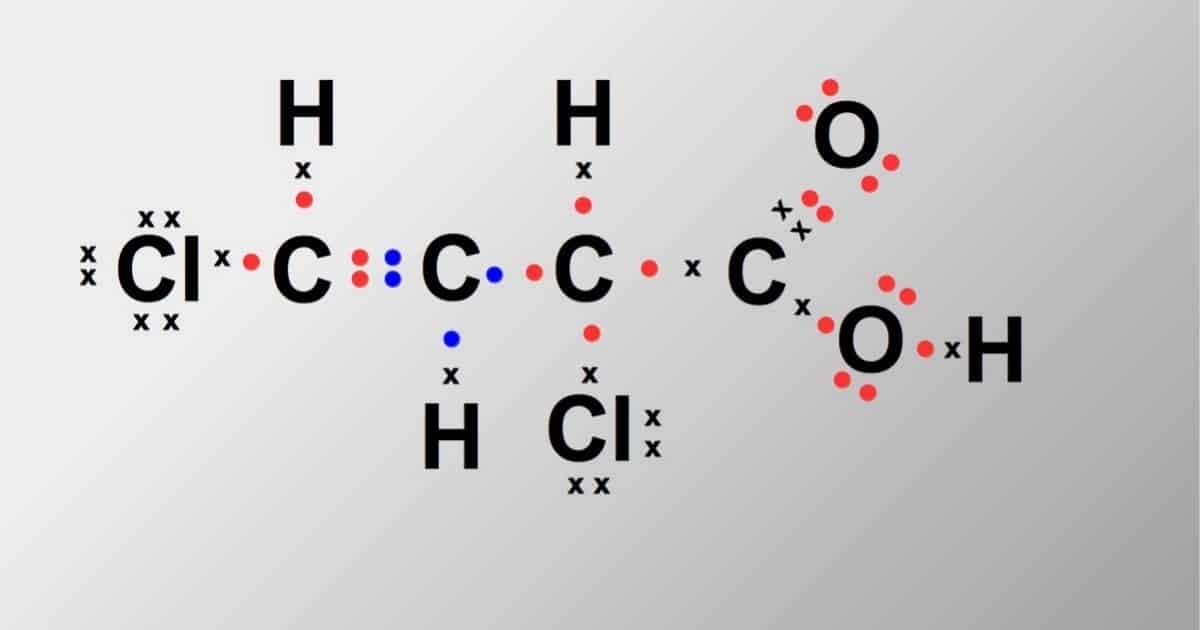
La estructura de Lewis fue introducida en 1916 por Gilbert Newton Lewis. Esta estructura es una representación gráfica que muestra la ubicación de electrones de valencia en una molécula y los respectivos enlaces covalentes.
Los enlaces covalentes son aquellos enlaces que se dan entre electrones compartidos entre dos átomos.
Ahora bien, los electrones de valencia que se representan en el diagrama de Lewis son los electrones que se ubican en la capa superior del átomo.
Esta estructura se basa principalmente en la regla del octeto. Esta regla, propia de la química, refleja la propiedad de los átomos de tener 8 electrones en el último nivel de energía. Compartir electrones ayuda a que los átomos cumplan este propósito y alcancen así estabilidad.
El diagrama de punto, como también se le llama, sirve, entonces, para conocer la estabilidad de la molécula, los elementos que la componen y cómo interactúan estos con otros elementos.
¿Cómo es la estructura de Lewis? Pasos para construirla
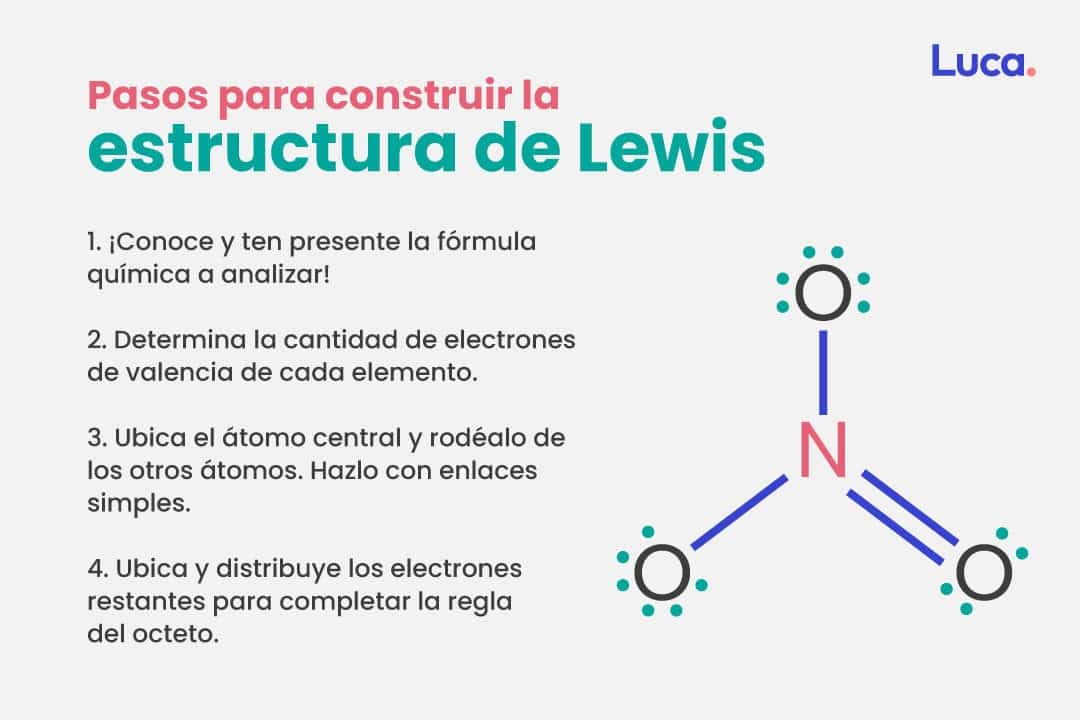
- El primer paso para empezar a construir la estructura de Lewis es conocer la fórmula química del compuesto a analizar.
- Luego, se determinan los electrones de valencia, pero ¿cómo? Bueno, tan solo se identifica a qué grupo pertenecen cada uno de los elementos. Por ejemplo: sí un elemento pertenece al grupo 1 o 2 poseen esta cantidad de electrones de valencia. Si, por el contrario, pertenecen al grupo 13 o 15, poseen 3 y 5 electrones de valencia respectivamente.
- En seguida se debe determinar el átomo central, es decir, el más electropositivo. Se rodea el átomo central de los otros átomos, con enlace simple.
- Los enlaces simples comparten dos electrones cada uno. Se debe entonces ubicar los electrones restantes.
- Distribuir los pares de electrones para completar el octeto.
Estructura de Lewis ejemplos: Porque la práctica es siempre la mejor guía
A continuación, conocerás dos ejemplos de estructura de Lewis con elementos muy conocidos.
- Estructura de Lewis CO2
Se debe partir por saber que en esta estructura hay dos átomos de oxigeno y un átomo de carbono.
El átomo central es el carbono. Se deberá entonces, ubicar los oxígenos a lado y lado del carbono con enlaces simples.
Los electrones totales de la molécula son 16. Este resultado se obtiene de sumar 6 electrones de cada oxígeno (12) + 4 electrones de carbono. De esta manera, cada átomo se deberá rodear de ocho electrones. A los dos hidrógenos se le ubican 6 más en forma de punto (ya tiene dos con el enlace simple).
Como el carbono solo tiene 4 con los dos enlaces, se convierte el enlace simple en doble con cada hidrógeno, completando así la regla del octeto.

2. Estructura de Lewis H2O
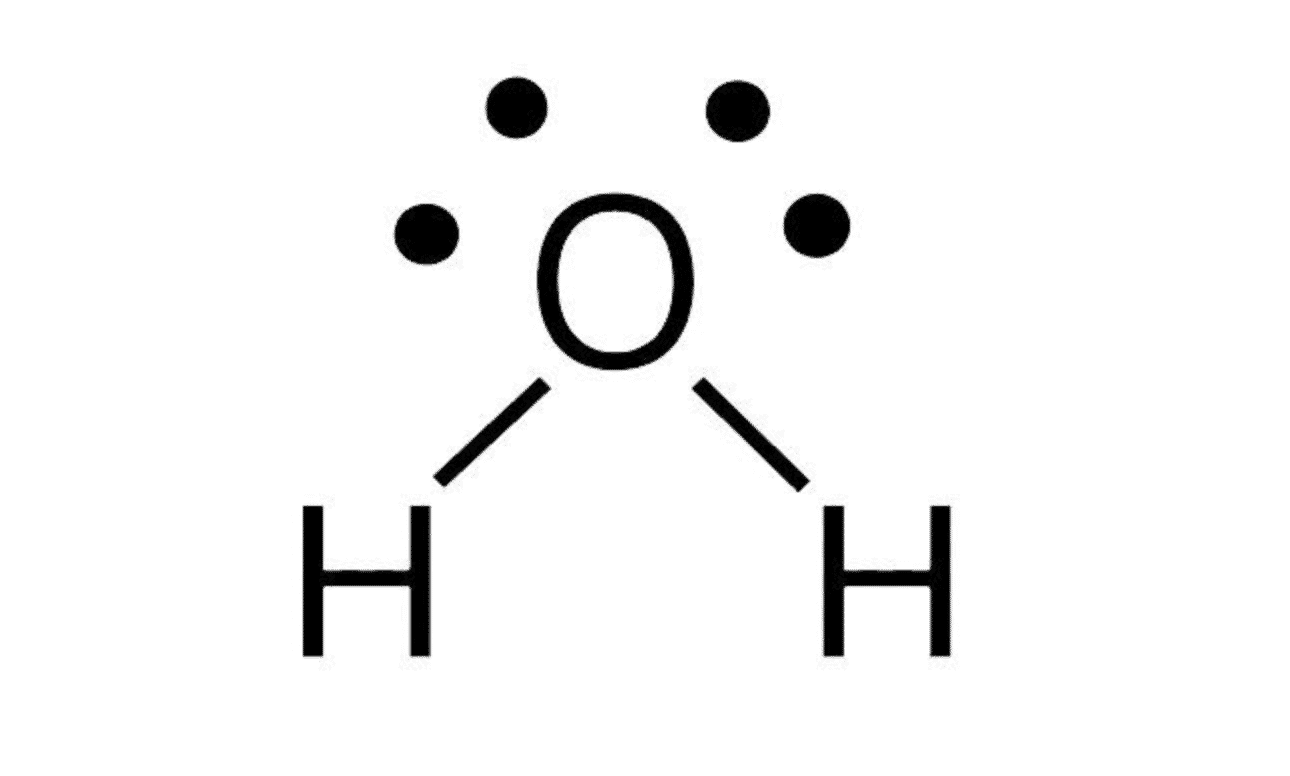
El átomo central es el oxígeno que comparte sus seis electrones con el hidrógeno. Este último solo tiene un electrón.
El oxígeno hace la compartición a través de dos enlaces simples. Esto debido a que el hidrógeno es una excepción de la regla del octeto y alcanza estabilidad con dos electrones únicamente. Quedando la estructura de Lewis así:
Conclusión
Como se mencionó anteriormente, la estructura de Lewis es un tema que se trabaja a lo largo de la educación secundaria. Aún así, tener presente las principales herramientas para el desarrollo de habilidades químicas desde la educación en la infancia otorgará aprendizajes clave para facilitar el proceso a largo plazo.
En Luca hemos creado una plataforma virtual de aprendizaje que cuenta con una malla curricular completa en las materias principales y que busca que los niños y jóvenes se formen conscientemente y disfruten del conocimiento. Para que conozcas más, no dudes en venir a visitarnos.


